Ce este IAD în chimia modernă
Hai să vorbim despre ce ISI în sinteza organică și anorganică.
definirea procesului
Sub reacții redox implică procese ca urmare a ceea ce se va schimba starea de oxidare a două sau mai multe elemente chimice în substanțe complexe sau simple.

Ce este oxidarea
Sub o astfel de oxidare se înțelege o reacție chimică în care un atom sau ion specific pierde electroni, reducând astfel numărul de oxidare inițială. Acest proces este caracteristic metalelor.
Ce este recuperarea
In cadrul procesului de recuperare implică o transformare chimică, având ca rezultat gradul de oxidare va reduce ionul sau o substanță simplă, adăugarea de electroni are loc. Această reacție este caracteristic nemetale și reziduuri acide.

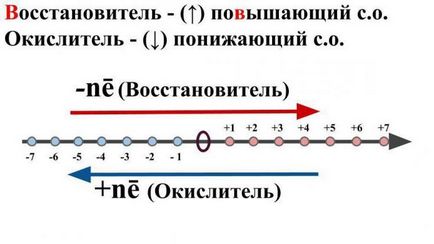
Caracteristică reducătorului
Având în vedere problema a ceea ce este IAD, nu putem ignora un astfel de lucru ca un „agent de reducere“.
Aceasta se referă la o moleculă neutră sau ion încărcat, care, ca rezultat al interacțiunii chimice va favoriza ion la un alt atom sau electron, crescând astfel gradul de oxidare.
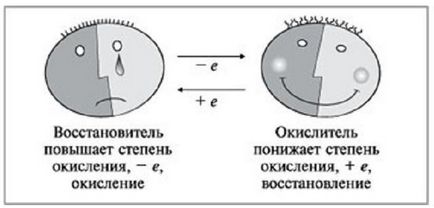
Determinarea conținutului de oxidant
Raționament asupra a ceea ce OVR este, de asemenea, important de menționat un termen cum ar fi „comburantului“. Sub aceasta se înțelege ioni sau atomi neutri care prin interacțiunea chimică va lua electroni negativi ai altor atomi sau particule neutre. În același timp, starea de oxidare inițială va scădea.
Argumentând asupra a ceea ce IAD, trebuie remarcat faptul despre soiurile acestor procese, care sunt adesea considerate în sinteza organică și anorganică.
interacțiunile intermoleculare implică astfel de procese în care atomii și un agent agent de reducere și oxidare sunt localizate în diferite materii prime este pus în reacție. Ca exemplu al acestui tip de transformare poate avea ca rezultat o interacțiune între oxid de mangan (4) și o soluție de acid clorhidric, în care se formează clor gazos, clorură de manganoase și apă.
In acest proces chimic apar ca reducător anioni de oxidare clor ca interacțiune. cation de mangan (oxidare starea 4) prezintă în capacitatea de reacție de oxidare, luând doi electroni, este redus.
interacțiunea intramoleculară este o astfel de transformări chimice, ca un agent de reducere și care atomii și oxidant sunt inițial atomi de o substanță de pornire, iar după conversie acestea sunt în diferitele produse de reacție.
Ca un exemplu de acest tip de reacție poate fi reprezentat printr-o descompunere a clorat de potasiu. După încălzirea substanței va fi transformată în clorură de potasiu și oxigen. Proprietățile oxidative sunt caracteristice anion cloratul, care, luând cinci electroni în reacție se va recupera transformata in clorura.
În acest caz, anionul de oxigen va prezenta proprietăți de reducere, sunt oxidate la oxigen molecular. Deci, ceea ce este IAD în acest caz? Acest proces de transfer de electroni între ioni, ceea ce duce la formarea celor două produse de reacție.
De asemenea, pentru acest tip de reacții chimice care au loc odată cu schimbarea de oxidare afirmă elemente sunt inițial într-o formulă se referă procesul de descompunere a nitritului de amoniu. Azot în picioare în cationul de amoniu având starea de oxidare 3, în timpul procesului trimite un șase electroni și este oxidat la azot molecular. Și azotul care este un membru al nitrit, primește șase electroni, cu un agent reducător, iar în timpul reacției este oxidat.
Ce este IAD în chimie? Definiția considerat de mai sus arată că această transformare asociată cu modificări în mai multe elemente de oxidare.
Autooxidare și recuperare (disparitate) presupune astfel de procese în cursul cărora ca agent de reducere și agentul de oxidare servește un atom de pornire care va crește și, simultan, reduce starea de oxidare, după terminarea reacției. Argumentând asupra a ceea ce IAD este în chimie, exemple de astfel de transformări pot fi găsite chiar și în cursul chimie de liceu. Sulfit de potasiu se descompune la încălzirea are ca rezultat formarea celor două săruri metalice: sulfuri și sulfat. Sulful în starea de oxidare +4 și de reducere și oxidare prezintă proprietăți prin ridicarea și coborârea indicatorilor de stare de oxidare.
Pentru a înțelege ce înseamnă WRA în chimia, noi numim o altă formă de astfel de transformări chimice. Kontrproportsionirovanie implică procese ca rezultat al cărui oxidant și atomii sunt compuse din reducător diferite componente de pornire, dar pe partea dreapta, ele formează un produs de reacție. De exemplu, prin reacția unui oxid de sulf (4) cu hidrogen sulfurat pentru a forma sulf și apă. Ion de sulf în stare de oxidare 4 va avea patru electroni, iar ionul de sulf cu indicator -2 pierde doi electroni. Ca rezultat, ambele dintre ele sunt transformate într-o substanță simplă, care are o stare de oxidare zero.

concluzie
Având în vedere problema a ceea ce este ISI în chimie, observăm că această conversie multiplă, prin care funcția de organisme vii, de a plasa o varietate de procese și fenomene naturale. Pentru a aranja ecuațiile în astfel de factori, este necesar să se facă un cântar electronic.
